
|
|
|||||
|
||||||
國家藥監局通報3家醫療器械生產企業飛檢情況摘要:
醫藥網6月5日訊 近日,國家藥品監督管理局通報對重慶欣汶醫療器械有限公司、長沙精通醫療器械有限公司、海南泰合醫療科技有限公司這3家醫療器械生產企業的飛行檢查結果。
國家藥品監督管理局關于重慶欣汶醫療器械有限公司停產整改的通告
(2018年第36號)
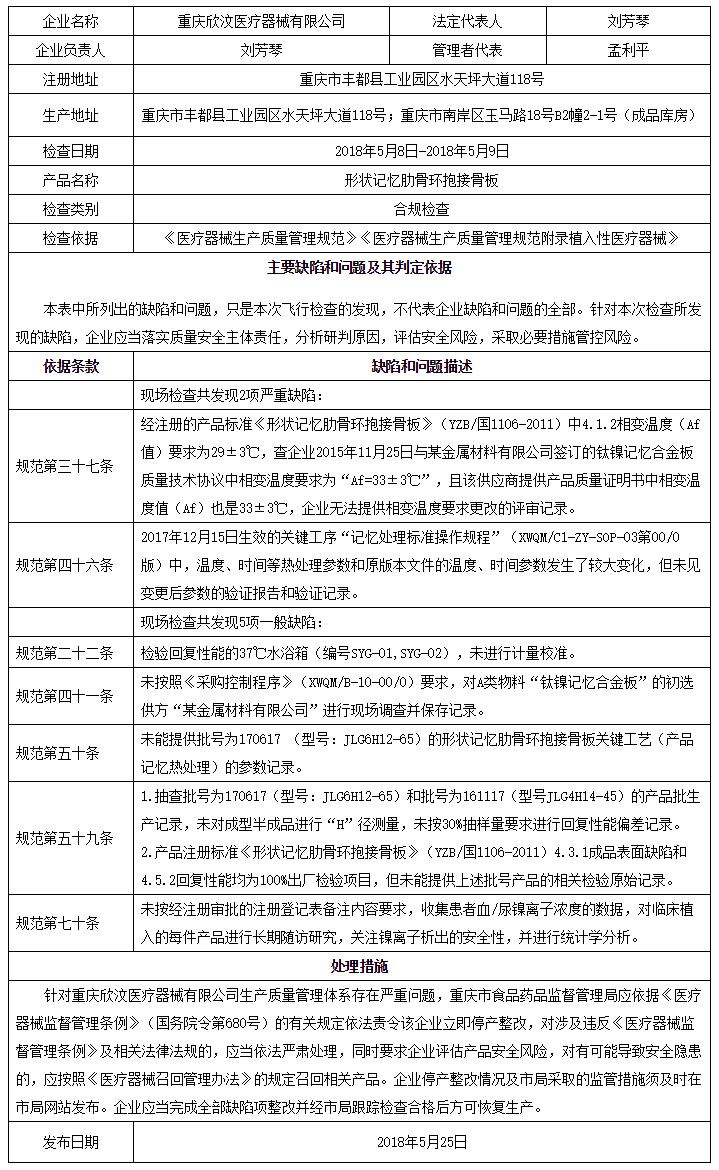
近期,國家藥品監督管理局組織對重慶欣汶醫療器械有限公司進行了飛行檢查。檢查中,發現該企業質量管理體系主要存在以下缺陷:
一、廠房與設施方面
企業檢驗回復性能的37℃水浴箱(編號SYG-01,SYG-02),未進行計量校準,不符合《醫療器械生產質量管理規范》(以下簡稱《規范》)中企業應當建立檢驗儀器和設備的使用記錄,記錄內容包括使用、校準、維護和維修等情況的要求。
二、設計開發方面
企業經注冊的產品標準《形狀記憶肋骨環抱接骨板》(YZB/國1106-2011)中4.1.2相變溫度(Af值)要求為29±3℃,查企業與某金屬材料有限公司簽訂的鈦鎳記憶合金板質量技術協議中相變溫度要求為“Af=33±3℃”,且該供應商提供產品質量證明書中相變溫度值(Af)也是33±3℃,企業無法提供相變溫度要求更改的評審記錄,不符合《規范》中企業應當對設計和開發的更改進行識別并保持記錄。必要時,應當對設計和開發更改進行評審、驗證和確認,并在實施前得到批準的要求。
三、采購方面
企業未按照《采購控制程序》(XWQM/B-10-00/0)要求,對A類物料“鈦鎳記憶合金板”的初選供方“某材料有限公司”進行現場調查并保存記錄,不符合《規范》中企業應當建立供應商審核制度,并應當對供應商進行審核評價。必要時,應當進行現場審核的要求。
四、生產管理方面
(一)現場查看企業2017年12月15日生效的關鍵工序“記憶處理標準操作規程”(XWQM/C1-ZY-SOP-03第00/0版)中,溫度、時間等熱處理參數和原版本文件的溫度、時間參數發生了較大變化,但未見變更后參數的驗證報告和驗證記錄,不符合《規范》中企業應當編制生產工藝規程、作業指導書等,明確關鍵工序和特殊過程的要求。
(二)企業未能提供批號為170617(型號JLG6H12-65)的形狀記憶肋骨環抱接骨板關鍵工藝(產品記憶熱處理)的參數記錄,不符合《規范》中每批(臺)產品均應當有生產記錄,并滿足可追溯要求的要求。
五、質量控制方面
抽查產品批號為170617(型號JLG6H12-65)和產品批號為161117(型號JLG4H14-45)的批生產記錄,企業未對成型半成品進行“H”徑測量,未按30%抽樣量要求進行回復性能偏差記錄;產品注冊標準《形狀記憶肋骨環抱接骨板》(YZB/國1106-2011)4.3.1成品表面缺陷和4.5.2回復性能均為100%出廠檢驗項目,但未能提供上述批號產品的相關檢驗原始記錄,不符合《規范》中每批(臺)產品均應當有檢驗記錄,并滿足可追溯要求的要求。
六、不良事件監測、分析和改進方面
企業未按經注冊審批的注冊登記表備注內容要求,收集患者血/尿鎳離子濃度的數據,對臨床植入的每件產品進行長期隨訪研究,關注鎳離子析出的安全性,并進行統計學分析,不符合《規范》中企業應當建立數據分析程序,收集分析與產品質量、不良事件、顧客反饋和質量管理體系運行有關的數據,驗證產品安全性和有效性,并保持相關記錄的要求。
企業已對上述其質量管理體系存在的缺陷予以確認。該企業上述行為不符合醫療器械生產質量管理規范相關規定,生產質量管理體系存在嚴重缺陷,國家藥品監督管理局責成重慶市食品藥品監督管理局依法責令該企業立即停產整改,對涉及違反《醫療器械監督管理條例》(國務院令第680號)及相關法律法規的,依法嚴肅處理。同時責成重慶市食品藥品監督管理局要求該企業評估產品安全風險,對有可能導致安全隱患的,應按照《醫療器械召回管理辦法》(國家食品藥品監督管理總局令第29號)的規定,召回相關產品。
待企業完成全部項目整改并經所在地省級食品藥品監督管理局跟蹤復查合格后方可恢復生產。
附件
 國家藥品監督管理局關于長沙市精通醫療器械有限公司停產整改的通告
(2018年第37號)
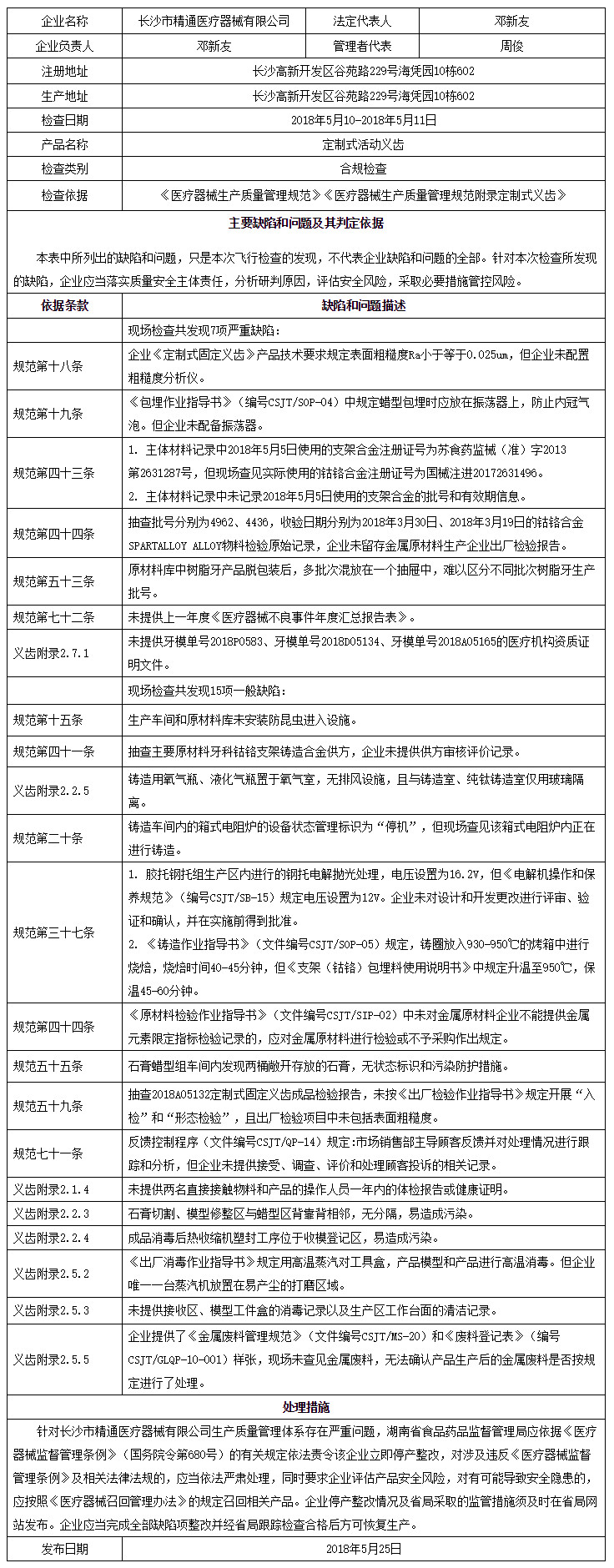
近期,國家藥品監督管理局組織對長沙市精通醫療器械有限公司進行了飛行檢查。檢查中,發現該企業質量管理體系主要存在以下缺陷:
一、廠房與設施方面
(一)企業《定制式固定義齒》產品技術要求規定表面粗糙度Ra小于等于0.025μm,但企業未配置粗糙度分析儀,不符合《醫療器械生產質量管理規范》及相關《附錄》(以下簡稱《規范》)中企業應當配備與產品生產規模、品種、檢驗要求相適應的檢驗場所和設施的要求。
(二)企業鑄造用氧氣瓶、液化氣瓶置于氧氣室,無排風設施,且與鑄造室、純鈦鑄造室僅用玻璃隔離,不符合《規范》中易燃、易爆、有毒、有害的物料應當專區存放、標識明顯,專人保管和發放的要求。
二、設備方面
企業《包埋作業指導書》(編號CSJT/SOP-04)中規定蠟型包埋時應放在振蕩器上,防止內冠氣泡,但企業未配備振蕩器,不符合《規范》中企業應當配備與所生產產品和規模相匹配的生產設備、工藝裝備等,并確保有效運行的要求。
三、設計開發方面
企業膠托鋼托組生產區內進行的鋼托電解拋光處理,電壓設置為16.2V,但《電解機操作和保養規范》(編號CSJT/SB-15)規定電壓設置為12V,《鑄造作業指導書》(文件編號CSJT/SOP-05)規定,鑄圈放入930—950℃的烤箱中進行燒焙,燒焙時間40—45分鐘,但《支架(鈷鉻)包埋料使用說明書》中規定升溫至950℃,保溫45—60分鐘,不符合《規范》中企業應當對設計和開發的更改進行識別并保持記錄,必要時,應當對設計和開發更改進行評審、驗證和確認,并在實施前得到批準的要求。
四、采購方面
(一)企業主體材料記錄中2018年5月5日使用的支架合金注冊證號為蘇食藥監械(準)字2013第2631287號,但現場查見實際使用的鈷鉻合金注冊證號為國械注進20172631496,主體材料記錄中未記錄2018年5月5日使用的支架合金的批號和有效期信息,不符合《規范》中采購記錄應當滿足可追溯的要求。
(二)抽查批號分別為4962、4436,收驗日期分別為2018年3月30日、2018年3月19日的鈷鉻合金 SPARTALLOY ALLOY物料檢驗原始記錄,企業未留存金屬原材料生產企業出廠檢驗報告,不符合《規范》中企業應當對采購物品進行檢驗或者驗證,確保滿足生產的要求。
五、生產管理方面
企業原材料庫中樹脂牙產品脫包裝后,多批次混放在一個抽屜中,難以區分不同批次樹脂牙生產批號,不符合《規范》中企業應當建立產品的可追溯程序,規定產品追溯范圍、程度、標識和必要的記錄的要求。
六、銷售和售后服務方面
企業未提供牙模單號2018P0583、牙模單號2018D05134、牙模單號2018A05165的醫療機構資質證明文件,不符合《規范》中應當選擇具有合法資質的醫療機構,保存醫療機構執業資質證明文件,并建立檔案的要求。
七、不良事件監測、分析和改進方面
企業未提供上一年度《醫療器械不良事件年度匯總報告表》,不符合《規范》中企業應當按照有關法規的要求建立醫療器械不良事件監測制度,開展不良事件監測和再評價工作,并保持相關記錄的要求。
企業已對上述其質量管理體系存在的缺陷予以確認。該企業上述行為不符合醫療器械生產質量管理規范相關規定,生產質量管理體系存在嚴重缺陷,國家藥品監督管理局責成長沙市精通醫療器械有限公司依法責令該企業立即停產整改,對涉及違反《醫療器械監督管理條例》(國務院令第680號)及相關法律法規的,依法嚴肅處理。同時責成湖南省食品藥品監督管理局要求該企業評估產品安全風險,對有可能導致安全隱患的,應按照《醫療器械召回管理辦法》(國家食品藥品監督管理總局令第29號)的規定,召回相關產品。
待企業完成全部項目整改并經所在地省級食品藥品監督管理局跟蹤復查合格后方可恢復生產。
附件
 國家藥品監督管理局關于海南泰合醫療科技有限公司停產整改的通告
(2018年第38號)
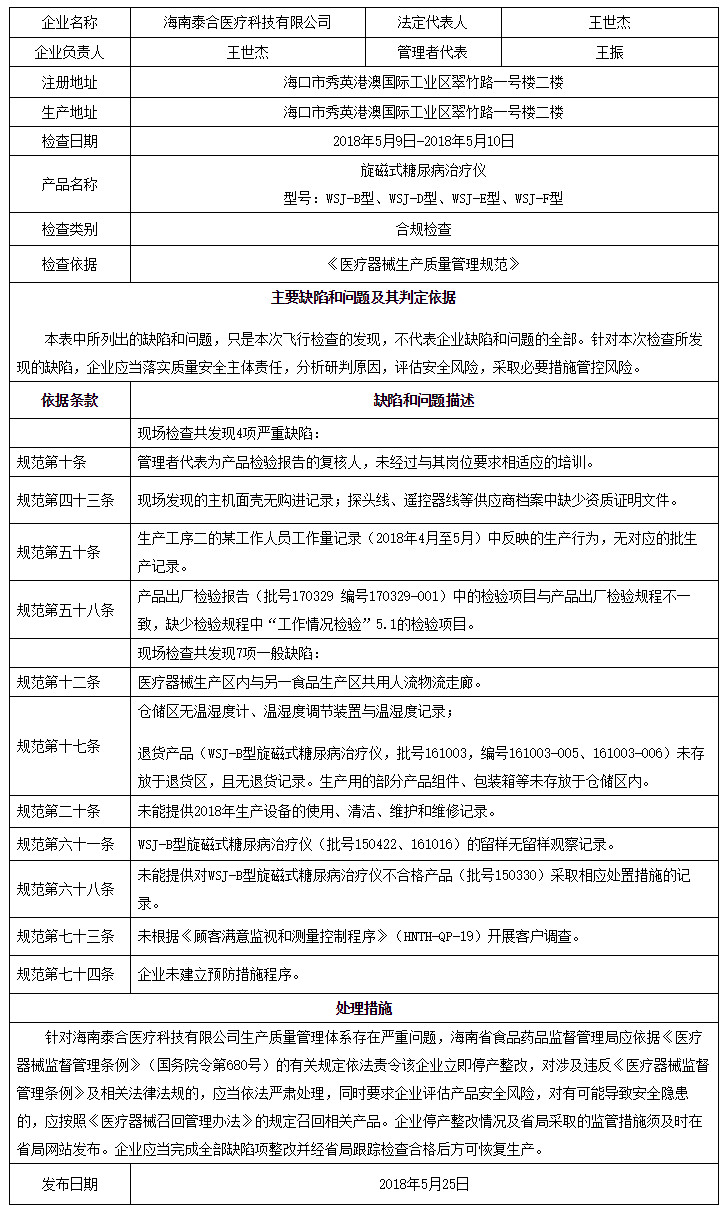
近期,國家藥品監督管理局組織對海南泰合醫療科技有限公司進行了飛行檢查。檢查中,發現該企業質量管理體系主要存在以下缺陷:
一、機構與人員方面
企業管理者代表為產品檢驗報告的復核人,未經過與其崗位要求相適應的培訓,不符合《醫療器械生產質量管理規范》及相關《附錄》(以下簡稱《規范》)中從事影響產品質量工作的人員,應當經過與其崗位要求相適應的培訓,具有相關理論知識和實際操作技能的要求。
二、廠房與設施方面
企業醫療器械生產區內與另一食品生產區共用人流物流走廊,不符合《規范》中廠房與設施應當符合生產要求,生產、行政和輔助區的總體布局應當合理,不得互相妨礙的要求。
三、采購方面
現場發現企業產品的主機面殼無購進記錄,探頭線、遙控器線等供應商檔案中缺少資質證明文件,不符合《規范》中應當建立采購記錄,包括采購合同、原材料清單、供應商資質證明文件、質量標準、檢驗報告及驗收標準等,采購記錄應當滿足可追溯的要求。
四、生產管理方面
(一)企業生產工序二的某工作人員工作量記錄(2018年4月至5月)中反映的生產行為,無對應的批生產記錄,不符合《規范》中每批(臺)產品均應當有生產記錄,并滿足可追溯的要求。
(二)企業產品出廠檢驗報告(批號170329編號170329-001)中的檢驗項目與產品出廠檢驗規程不一致,缺少檢驗規程中“工作情況檢驗”5.1的檢驗項目,不符合《規范》中企業應當根據強制性標準以及經注冊或者備案的產品技術要求制定產品的檢驗規程,并出具相應的檢驗報告或者證書的要求。
五、不合格品控制方面
企業未能提供對WSJ-B型旋磁式糖尿病治療儀不合格產品(批號150330)采取相應處置措施的記錄,不符合《規范》中企業應當對不合格品進行標識、記錄、隔離、評審,根據評審結果,對不合格品采取相應的處置措施的要求。
企業已對上述其質量管理體系存在的缺陷予以確認。該企業上述行為不符合醫療器械生產質量管理規范相關規定,生產質量管理體系存在嚴重缺陷,國家藥品監督管理局責成海南泰合醫療科技有限公司依法責令該企業立即停產整改,對涉及違反《醫療器械監督管理條例》(國務院令第680號)及相關法律法規的,依法嚴肅處理。同時責成海南省食品藥品監督管理局要求該企業評估產品安全風險,對有可能導致安全隱患的,應按照《醫療器械召回管理辦法》(國家食品藥品監督管理總局令第29號)的規定,召回相關產品。
待企業完成全部項目整改并經所在地省級食品藥品監督管理局跟蹤復查合格后方可恢復生產。
 |
|
Copyright ?2015 廣東穗康醫藥有限公司
粵ICP備15022662號(粵)
-技術支持:信息管理部|聯系我們
|